Tidigare behöver inte vara bättre
Viktiga budskap
- Tidig diagnos behöver inte leda till bättre hälsa; ibland blir det tvärtom.
- Screening bör bara införas om det finns tillräckliga belägg för att det gör nytta.
- Att inte starta ett screeningprogram är ibland det bästa alternativet.
- Personer som erbjuds screening måste få saklig information om både för- och nackdelar.
- När nya screeningprogram föreslås överdriver man ofta nyttan medan riskerna tonas ner eller förbises.
- Mycket hänger på att både nyttan och riskerna med screening förmedlas på ett bra sätt.
I de tre första kapitlen har vi visat att behandlingar som inte utsatts för tillräcklig vetenskaplig prövning kan göra stor skada. Nu kommer vi att rikta uppmärksamheten mot så kallad screening, det vill säga massundersökningar av till synes friska människor för att hitta tidiga tecken på sjukdom. Tanken kan ju låta vettig – det måste väl vara bättre att försöka förebygga att drabbas av en svår sjukdom och hålla sig frisk? Inte nödvändigtvis. Även om screening av några sjukdomar är bra, finns det också en risk att massundersökningar gör skada.
I det här kapitlet ger vi exempel på varför det ofta – men inte alltid – kan vara bra att få en diagnos tidigt. Vi visar att många typer av screening inte gör nytta, eller att nyttan med dem är oklar. Vi diskuterar också hur fördelarna med screening ofta överdrivs, medan riskerna tonas ner eller förbises.
Screening kommer alltid att förvandla vissa människor som testar ’positivt’ från personer till patienter, något som inte bör ske utan vidare. När en patient söker hjälp, gör läkaren sitt bästa. Att läkarvetenskapen har brister kan vi inte klandra doktorn för. Situationen är en helt annan när en läkare tar initiativ till screening. Enligt vår uppfattning borde det då krävas klara bevis för att en betydande andel av dem som screenas får ett annat sjukdomsförlopp.”
Cochrane AL, Holland WW. Validation of screening procedures. British Medical Bulletin 1971;27:3–8.
Screening av friska människor får aldrig göras lättvindigt. Det finns viktiga nackdelar att tänka på. Undersökningen i sig är en medicinsk åtgärd, liksom att kalla människor till screening. Många som väljer att tacka nej går omkring med ett gnagande tvivel om det verkligen var ”rätt” beslut; det är ju ganska naturligt. Hade man aldrig fått något erbjudande om screening, skulle läget ha varit helt annorlunda.
Screening som syftar till att ge lugnande besked eller leda vidare till behandling bör på sin höjd erbjudas friska människor när det finns vetenskapligt stöd för att undersökningen (a) gör mer nytta än skada, till en rimlig kostnad, och (b) ingår i ett väl utformat och väl genomfört åtgärdsprogram (se nedan under avsnittet Syftet med screening och varför det behövs vetenskapligt stöd).[1]
Screening är mycket mer än ett enstaka test. Personer som bjuds in till undersökning måste få tillräckligt med opartisk och relevant information för att bestämma om de ska tacka ja eller nej – det vill säga, de måste få veta vad de utsätter sig för (se nedan).[2]
Så här borde man egentligen se på screening:
Screening = en undersökning plus ett effektivt åtgärdsprogram
Lärdomar av screening för neuroblastom
Erfarenheterna av screening för neuroblastom, en sällsynt cancersjukdom som främst drabbar små barn, ger flera viktiga lärdomar. Tumören drabbar nervceller i olika delar av kroppen. Överlevnadschanserna för de drabbade barnen beror på sådant som tumörens läge, hur spridd den är när den påvisas och barnets ålder. Kring 55 procent av de barn som är mellan ett och fyra år när diagnosen ställs lever i ytterligare fem år.[3] Det speciella med neuroblastom (och några andra cancersjukdomar) är att sjukdomen ibland försvinner helt utan behandling, något som kallas spontan remission.[4]
Neuroblastom var en intressant kandidat för screening av fyra skäl:
1. Barn som får diagnosen före ett års ålder klarar sig bättre än de som får den senare.
2. Barn som har tidiga stadier av sjukdomen klarar sig mycket bättre än barn med långt framskriden sjukdom.
3. Det finns en enkel och billig undersökningsmetod där man tar prov från våta blöjor och mäter ämnen i urinen.
4. Undersökningen upptäcker nio av tio barn med neuroblastom.[5]
Japan var först med att 1985 införa massundersökning av neuroblastom hos spädbarn, vid sex månaders ålder. Detta gjordes trots att det saknades välgjorda studier som visade på någon nytta. Under landets första tre år med screening ställdes diagnosen på 337 barn, varav 97 procent levde 1990 efter att ha fått behandling. Tjugo år senare fanns det fortfarande inget vetenskapligt stöd för att screeningen skulle ha räddat några av barnen till livet. Hur kan det komma sig?
När man granskade faktaunderlaget för att starta och lansera screeningen i Japan fann man allvarliga brister, och en tydlig förklaring. Den imponerande överlevnadssiffran 97 procent beror på den typ av systematiska fel (bias) som på fackspråk kallas långvarighetsfel. Det innebär att screening oftare påvisar tillstånd som utvecklas under lång tid (i det här fallet långsamt växande tumörer). Däremot är det mindre sannolikt att snabbväxande tumörer upptäcks med screening. Sådana tumörer leder i stället till symtom hos barnet, till exempel buksvullnad, som snabbt upptäcks. De här snabbväxande tumörerna kan vara mycket allvarligare än de som växer långsamt. Prognosen för långsamt växande neuroblastom är oftast god, bland annat för att tumörerna försvinner av sig själva (se ovan).[6]
De flesta av de 337 barn som fick diagnosen med hjälp av screening skulle sannolikt ha klarat sig bra även utan något screeningprogram, och de barn som verkligen hade en allvarlig form av sjukdomen fanns aldrig med bland de fall som upptäcktes. Dessutom påvisade screeningen antagligen en del tumörer som skulle ha försvunnit av sig själva, i vilket fall som helst – och utan screening skulle man ha sluppit veta om dem. Den överdiagnostik som screeningen ledde till förvandlade barnen till patienter och utsatte dem i onödan för risker med behandling.
Dessutom visade det sig att de lovande små studier som screeningen i Japan byggde på hade beräknat livslängden från det datum då diagnosen ställdes, och inte från barnets födelsedatum. Detta är ett problem, för det är inte säkert att patienter lever längre bara för att sjukdomen upptäcks tidigare: de kanske bara lever längre tid med etiketten ”sjuk”. För att uttrycka det annorlunda: det kan se ut som om patienten lever längre eftersom ”tidtagaruret” för sjukdomen sätts igång tidigare. Detta är ett exempel på en annan typ av vetenskaplig fälla som på engelska kallas ”lead time bias”, ett fel som kan undvikas om man mäter överlevnad från födelsedatum i stället för datum då diagnosen ställs.
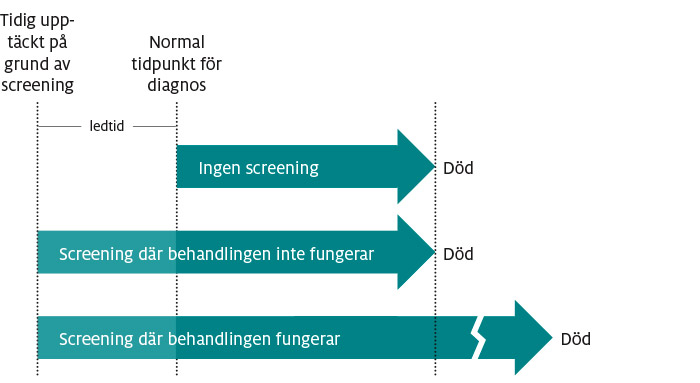
Figur 4. Att leva fler år med en sjukdomsstämpel eller att få ett längre liv
När forskarna slutligen fick tillgång till resultat från välgjorda kanadensiska och tyska studier av totalt cirka tre miljoner barn, visade screeningen inga hälsovinster utan tvärtom tydliga skadeverkningar.[7] Det handlade om omotiverade operationer och cytostatikabehandlingar, båda med risk för svåra biverkningar. Japan upphörde därför med screening för neuroblastom bland spädbarn år 2004.
UTGÅ INTE FRÅN ATT TIDIG UPPTÄCKT ÄR BÄTTRE
Screening för neuroblastom illustrerar hur lätt man kan luras att tro att screening måste vara bra bara för att en sjukdom kan upptäckas tidigt […] De två studierna visar inte bara att det var meningslöst med screening för neuroblastom, utan att det också ledde till en ”överdiagnostik” – upptäckt av tumörer som skulle ha gått tillbaka av sig själva. I båda studierna fick barnen allvarliga komplikationer av behandlingen […] Förhoppningsvis kan man dra lärdom av detta när man överväger att genomföra andra screeningprogram, till exempel för prostatacancer.”
Morris JK. Screening for neuroblastoma in children. Journal of Medical Screening 2002;9:56.
Efter de lovande tidiga studierna hade man på 1980-talet planerat att även småbarn i New South Wales i Australien skulle massundersökas för neuroblastom. De första resultaten visade som sagt att de undersökta barnen levde längre räknat från diagnosdatumet, men ingen hade undersökt deras överlevnad räknat från födelsedatumet. En australisk specialist ingrep och räknade om de japanska resultaten utifrån barnens födelsedatum. Analysen visade ingen skillnad i överlevnad mellan screenade och icke-screenade. Myndigheterna i New South Wales bestämde sig därmed för att inte genomföra screeningprogrammet. På så sätt slapp barnen onödig skada och hälso- och sjukvården onödiga utgifter.
![]() VEM BESLUTAR OM SCREENING I SVERIGE?
VEM BESLUTAR OM SCREENING I SVERIGE?
I Sverige tar Socialstyrelsen fram rekommendationer om nationella screeningprogram. Men det är upp till varje landsting att bestämma om och när ett screeningprogram ska startas. Att Socialstyrelsen gör rekommendationer för hela landet beror på att man vill skapa förutsättningar för en jämlik vård. Alla som omfattas av ett screeningprogram ska ha samma möjlighet att delta. Dessutom krävs det ett högt deltagande för att ett screeningprogram ska leda till bättre hälsa i befolkningen. Socialstyrelsen skriver att screening, liksom andra åtgärder inom hälso- och sjukvården, ska prioriteras med hänsyn till samhällets begränsade resurser. Det behövs en samlad bedömning av nytta, risker och kostnader. Myndigheten har tagit fram en modell för hur man ska bedöma, föra in och följa upp screeningprogram.
Källa: Socialstyrelsen
Att väga för- och nackdelar
Det finns många exempel på värdefulla screeningundersökningar. Den kanske vanligaste ”screeningen” för vuxna är den kontroll av riskfaktorer för hjärtsjukdom och stroke som görs en hel del inom till exempel företagshälsovård och primärvård. Det finns gott vetenskapligt stöd för att högt blodtryck, rökning och höga kolesterolnivåer i blodet ökar risken för dessa sjukdomar samt att man kan förhindra hjärtinfarkt och stroke genom att hitta riskfaktorerna, så att man kan ge råd till och behandla de människor som har dem.
Screening för fenylketonuri: uppenbara fördelar
Nyfödda testas rutinmässigt för den ärftliga sjukdomen fenylketonuri (PKU). Spädbarn med PKU kan inte bryta ner fenylalanin, ett ämne som finns i vanliga födoämnen som mjölk, kött, fisk och ägg. Om sjukdomen inte behandlas, ansamlas fenylalanin i blodet vilket leder till svår och obotlig hjärnskada. PKU-provet innebär att man tar några droppar blod från barnets häl, och låter provet analyseras på ett laboratorium. Om sticktestet är positivt och diagnosen kan bekräftas med ytterligare prover, behandlar man med specialkost, och det gör att barnet utvecklas normalt. I samma prov som man undersöker PKU, testar man även om barnet har vissa medfödda hormon- eller enzymsjukdomar som leder till stora problem om de inte behandlas på rätt sätt.
Screening för pulsåderbråck i buken: bedömningen viktig
I den andra änden av åldersskalan kan screening för bråck på aorta, stora kroppspulsådern, också vara värdefullt. Aorta går från hjärtat genom bröstkorgen och buken. Hos vissa personer försvagas kroppspulsådern med åldern, och blodådern börjar bukta ut inuti buken – detta kallas aneurysm, ett tillstånd som sällan ger några symtom och som är vanligast bland män från 65 år och uppåt. Stora aneurysm kan plötsligt brista och börja läcka utan förvarning, vilket oftast leder till döden.[8]
Eftersom det finns vetenskapligt stöd för att aneurysm kan förekomma hos äldre män kan det användas som utgångspunkt för att starta ett screeningprogram. I till exempel Storbritannien och i flera landsting i Sverige erbjuds män (men inte kvinnor) ultraljudsundersökning när de fyllt 65 år. Om undersökningen visar stora aneurysm får männen råd och behandling, oftast operation, hos specialist. Män med mindre aneurysm följs över tid med fler ultraljudskontroller, medan de som inte har något aneurysm inte behöver genomgå fler undersökningar. Operationen kan vara omfattande, och om andelen komplikationer är hög innebär det att fler män skadas än får hjälp. Kvaliteten på undersökningen och operationen är helt avgörande för nyttan.
Screening för bröstcancer: väl etablerad men upplägget är fortfarande omtvistat
En amerikansk folkhälsoexpert sa så här 2010: ”Ingen screeningundersökning har testats noggrannare än den för bröstcancer. Under de senaste 50 åren har mer än 600 000 kvinnor deltagit i tio randomiserade studier (med slumpmässig fördelning av deltagarna), alla med omkring tio års uppföljning. Med tanke på denna enorma forskningsinsats är det ironiskt att mammografi fortfarande är en av de mest omtvistade metoderna inom läkarvetenskapen.”[9]
Varför är mammografi så omtvistat? Mammografiundersökningar leder inte bara till tidig diagnos, utan också (i likhet med prostatacancerscreening, se nedan) till att man ibland hittar cancer som annars aldrig skulle ha upptäckts under patientens livstid. Det går inte heller att undvika att mammografiundersökningen i vissa fall ger falskt alarm, det vill säga man hittar ingen cancer vid ytterligare undersökningar som till exempel vävnadsprov. Av liknande skäl har man ifrågasatt kampanjer om att alla kvinnor själva ska undersöka brösten och vara uppmärksamma på förändringar.[10]
I samband med mammografi går det alltså inte på förhand att tala om vem som kommer att räddas till livet och vem som behandlas i onödan – och detta är i och för sig inget unikt för bröstcancer. Nästan allt vården gör innebär att människor behandlas ”för säkerhets skull”: friska blindtarmar tas bort för att undvika bukhinneinflammation hos patienter med misstänkt blindtarmsinflammation; alla med lunginflammation får antibiotika trots att många skulle ha tillfrisknat utan behandling; patienter med lymfkörtelcancer får upprepade cytostatikakurer trots att många är botade redan efter en eller två kurer. Att behandla somliga ”i onödan” är ofta oundvikligt när man försöker rädda liv. När det gäller mammografi kan man ganska väl uppskatta hur många liv som räddas. Svårigheten har främst varit att uppskatta skadan av att upptäcka och åtgärda vissa misstänkta förändringar på mammografi. Diskussionen är intressant. Författarna till en systematisk översikt anser att en del studier har överskattat mammografins effekt på dödligheten och att riskerna är betydande.[11]
Författarna är rädda för att friska kvinnor får cancerbehandlingar i onödan. De påpekar också att en hel del kvinnor kommer att få ett besked som i själva verket är ett falskt alarm. Den psykiska pressen kan vara stor innan kvinnan får veta om det är cancer eller inte – men även efteråt. Denna översikt har dock blivit kritiserad för att siffrorna i den bygger på osäkra antaganden.
I detta sammanhang är det också viktigt att komma ihåg att man inte behandlar bröstcancer enbart utifrån resultatet av mammografi. Man gör vävnadsprover eller andra undersökningar innan man påbörjar behandling. Även om för- och nackdelar med mammografiscreening debatteras, rekommenderas undersökningarna av de flesta expertgrupper runt om i världen. I Sverige rekommenderar Socialstyrelsen allmän screening av kvinnor i åldern 40–74 år. Motiven framgår av rutan nedan.
![]() VARFÖR REKOMMENDERAS KVINNOR MAMMOGRAFI I SVERIGE?
VARFÖR REKOMMENDERAS KVINNOR MAMMOGRAFI I SVERIGE?
Avgörande för rekommendationen är att screeningprogrammet sänker dödligheten i bröstcancer med 16–25 procent. En negativ effekt av programmet är dock att det finns en risk för att bröstcancer som inte skulle ha gett symtom diagnostiseras och behandlas i onödan. För ett fåtal personer kan det innebära att delar av eller hela bröstet opereras bort, trots att cancern aldrig skulle ha gett symtom under deras återstående livstid. Men bedömningen är att programmets hälsovinster i form av minskad dödlighet ändå överväger de negativa effekterna som innebär att hela eller delar av bröst opereras bort i onödan. Den hälsoekonomiska analysen visar att programmet har en måttlig kostnad per effekt, vilket innebär 100 000–500 000 kronor per vunnet kvalitetsjusterat levnadsår.
Källa: Socialstyrelsen
I Storbritannien har debatten om nytta och risker med bröstcancerscreening lett till att man har tillsatt en oberoende utredningsgrupp [12] som gjort en egen genomgång av studierna och uppskattningar av vad resultaten betyder för brittiska kvinnor idag. Bland 10 000 kvinnor i 50-årsåldern som under de närmaste 20 åren regelbundet bjuds in till mammografi, kommer mammografin att leda till att 129 kvinnor får en cancerdiagnos i onödan, medan 43 kvinnor med bröstcancer kommer att räddas till livet. Den här utredningens bedömning av de randomiserade studierna var att fördelarna med mammografi väger tyngre än nackdelarna.
Om rutinmässig screening ska rädda liv på samma sätt som i de kliniska studierna måste deltagandet vara högt, och de grupper som har mest nytta av screeningen måste komma till undersökningen. När ett antal kvinnor uteblir av ekonomiska eller praktiska skäl blir nyttan av massundersökningarna betydligt mindre, eftersom det är just dessa grupper som har mest att vinna på screening. Man kan således ha betydligt mer att förlora än att vinna på att till exempel avgiftsbelägga screening.
Screening för prostatacancer: uppenbara nackdelar och osäker nytta
Prostatacancer, den näst vanligaste cancerformen hos män globalt sett,[13] kan grovt sett delas in i två typer. En del män har en aggressiv form av sjuk- domen med snabb spridning och hög dödlighet. Men många har långsamt växande tumörer som aldrig kommer att medföra några hälsorisker under mannens livstid. I idealfallet skulle screening bara avslöja de allvarliga cancerformerna – i förhoppning om att de kan behandlas – men inte dem som växer långsamt. Behandlingen av all slags prostatacancer innebär risk för besvärande biverkningar i form av inkontinens och impotens, vilket kan vara ett högt pris att betala om sjukdomen utan behandling inte skulle ha medfört några problem.[14]
DILEMMAT MED ATT SÖKA EFTER PROSTATACANCER
Prostatacancer har beskrivits som det främsta exemplet på överdiagnostik. Detta innebär inte att det inte finns män som tack vare en tidig diagnos undgår en för tidig död i prostatacancer. Men […] vi har få möjligheter att på förhand veta vilka män som kommer att ha nytta av screening och vilka som kommer att behandlas i onödan, ofta med allvarliga negativa följder för livskvaliteten. Det grundläggande problemet när vi genomför screening och testar för prostatacancer är att vi hittar många fler fall än vi någonsin gjort förut, och även om det låter märkligt så skulle många av de här cancerfallen aldrig ha blivit livshotande. Förr skulle männen aldrig ha vetat om att de hade prostatacancer; de skulle till slut ha dött av någonting annat, med sin prostatacancer i stället för på grund av den. Genom att upptäcka alla dessa långsamt växande prostatatumörer ger vi många fler män diagnosen prostatacancer än någonsin förr. Det är detta som är ”överdiagnostik”. Detta är det stora dilemmat för alla män som överväger att låta sig testas.”
Chapman S, Baratt A, Stockler M. Let sleeping dogs lie? What men should know before getting tested for prostate cancer. Syndey: Sydney University Press, 2010: S.25.
De flesta män med prostatacancer har förhöjda nivåer av ett ämne i blodet som kallas prostataspecifikt antigen (PSA). Det finns emellertid inget exakt ”normalvärde” som skiljer en man med cancer från en som inte har cancer,[15] och så många som en av fem män med cancer som påverkar hälsan har normala PSA-värden. Och trots namnet är PSA allt annat än ”specifikt” – till exempel kan godartade prostatatumörer, infektioner och till och med vissa icke receptbelagda smärtlindrande mediciner ge förhöjda PSA-värden. Om man bara ser till detta har mätning av PSA-värdet uppenbara begränsningar som screeningmetod.
Ofta har läkare, patientgrupper och företag som säljer testen tryckt på för att införa allmän PSA-screening, vilket också har skett i många länder. Påtryckningarna för PSA-screening har varit särskilt intensiva i USA, där uppskattningsvis 30 miljoner män testas varje år eftersom man anser att det är förnuftigt att göra det. Vilket vetenskapligt stöd finns det då för att tidig upptäckt av prostatacancer med PSA-screening ger hälsovinster, och vad vet man om negativa effekter av testet?
MANNEN SOM UPPTÄCKTE PSA FÖRKLARAR
Testets popularitet har fått katastrofala följder för folkhälsan till enorma kostnader. Det är något som jag är smärtsamt medveten om, eftersom det var jag som upptäckte PSA 1970. […] I USA lägger man ner enorma summor på screening för prostatacancer. Den årliga notan för PSA-testen uppgår till minst tre miljarder dollar, och en stor del av detta ersätts av det offentligt finansierade sjukförsäkringssystemet Medicare och av det så kallade Veterans Administration under det amerikanska departementet för krigsveteraner.
Prostatacancer får mycket publicitet, men fundera lite på siffrorna: risken för amerikanska män att få diagnosen prostatacancer är 16 procent, men risken för att de ska dö av sjukdomen är bara 3 procent. Det beror på att de flesta prostatatumörer växer långsamt. Med andra ord: det är mer sannolikt att män som lyckas bli gamla dör med prostatacancer än av den. […] Jag har nu i många år försökt förklara att PSA inte påvisar cancer, och, vilket är ännu viktigare, PSA-testet skiljer inte mellan de båda typerna av prostatacancer – den man dör av och den man inte dör av.”
Ablin RJ. The great prostate mistake. New York Times, 10 mars 2010.
Det kommer alltmer tillförlitlig vetenskaplig dokumentation om fördelarna och nackdelarna med PSA. År 2010 gjordes en systematisk granskning av resultaten från alla relevanta studier. Utvärderingen visade att PSA-screening visserligen ökade sannolikheten för att få diagnosen prostatacancer (vilket var förväntat), men dödligheten i sjukdomen och dödligheten oavsett orsak påverkades inte markant.[16]
Är trenden alltså att man börjar ifrågasätta PSA-testningen? Richard Ablin, mannen som upptäckte PSA, har länge hävdat att man borde göra det. År 2010 skrev han, utifrån amerikanska förhållanden: ”Jag kunde aldrig drömma om att min upptäckt för fyrtio år sedan skulle leda till en sådan vinststyrd folkhälsokatastrof. Läkarvetenskapen måste inse fakta och stoppa felaktig användning av PSA-testning. Det skulle innebära besparingar på flera miljarder dollar och innebära att män slapp onödiga och skadliga behandlingar.” Åtminstone borde alla män få information om PSA-testets begränsningar och eventuella negativa konsekvenser innan de gör testet. En grupp specialister har sagt följande: ”[Män] borde få veta att testet inte kan säga om de har livshotande cancer, men att det kan leda till en mängd undersökningar och behandlingar som de kanske lika gärna kunde ha sluppit.”[17]
Frågan är kontroversiell – man måste väga en begränsad överlevnadsvinst hos en del män mot en betydande risk för besvärande biverkningar hos betydligt fler. I Sverige avråder Socialstyrelsen från allmän screening med PSA-prov. Skälen framgår av faktarutan på nästa sida.
![]() VARFÖR REKOMMENDERAS INTE PSA-SCREENING AV MÄN I SVERIGE?
VARFÖR REKOMMENDERAS INTE PSA-SCREENING AV MÄN I SVERIGE?
I Sverige har PSA-screening av män mellan 50 och 70 år diskuterats. Idag anger Socialstyrelsen att hälso- och sjukvården inte bör erbjuda screening för prostatacancer med test av prostataspecifikt antigen (PSA). Så här motiverar Socialstyrelsen rekommendationen:
”Avgörande för rekommendationen är att de negativa effekterna, i form av diagnostik och behandling av prostatacancer som egentligen inte skulle behöva behandlas, är så omfattande vid screening med PSA-test. Screeningprogrammet skulle kunna minska dödligheten i prostatacancer med 1 till 4 dödsfall per 1 000 män efter 10–15 år. Samtidigt skulle cirka 40–50 fler fall av prostatacancer diagnostiseras per 1 000 män, jämfört med om det inte hade förekommit någon screening.
De flesta som behandlas för prostatacancer får försämrad sexuell funktion, dessutom är urinläckage och ändtarmsbesvär tämligen vanliga bieffekter. Socialstyrelsen bedömer att de negativa effekterna i form av överdiagnostik och överbehandling väger tyngre på befolkningsnivå, än de positiva i form av minskad dödlighet och sjuklighet i prostatacancer. Därför har inte Socialstyrelsen gjort någon hälsoekonomisk bedömning av programmet.”
Källa: Socialstyrelsen
Screening för lungcancer: tidigt, men inte tillräckligt tidigt?
Screening kan leda till att sjukdomar upptäcks tidigare, men inte alltid så tidigt att det har någon betydelse (se figur 5).
Vissa cancerformer, till exempel lungcancer, kan spridas i kroppen innan patienten får symtom och innan några undersökningar kan påvisa förekomsten av cancer. De försök som gjorts för att upptäcka lungcancer med hjälp av röntgen kan illustrera det här problemet (se stadium B i figur 5). Flera stora studier av storrökare på 1970-talet visade att även om sjukdomen upptäcktes tidigare fanns det inget vetenskapligt stöd för att det ledde till minskad dödlighet i sjukdomen. De lungcancerfall som upptäcktes på röntgen hade redan spridits utanför lungorna. Dessa patienter levde alltså längre med sin cancerdiagnos, och de fick behandling tidigare, men det påverkade inte deras förväntade totala livslängd.
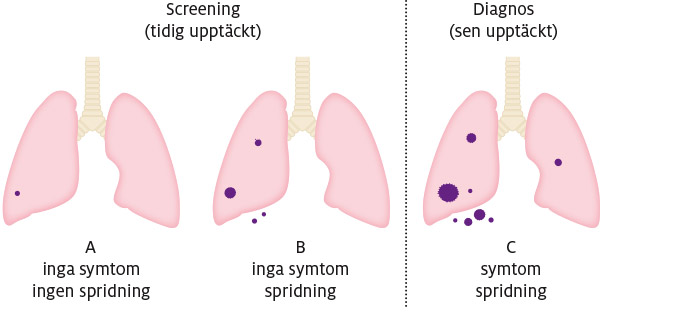
Figur 5. Tillväxt och spridning av lungcancer hos storrökare
I en senare stor randomiserad studie som omfattade 53 000 nuvarande och tidigare storrökare jämfördes röntgenscreening av lungor och bröstkorg och screening med en speciell typ av datortomografi (DT) som kallas spiral-DT. Båda grupperna genomgick tre årliga screeningomgångar. Spiral-DT gav diagnosen lungcancer på ett ännu tidigare stadium än röntgenbilder, och för en liten andel av patienterna var detta tillräckligt tidigt (stadium A i figur 5) för att behandlingen skulle göra nytta (354 dödsfall på grund av lungcancer i spiral-DT-gruppen jämfört med 442 i röntgengruppen). Men detta fördelaktiga resultat uppnåddes på bekostnad av att många människor felaktigt fick diagnosen lungcancer. Slutresultatet blev så här: av 1 000 storrökare som hade genomgått tre årliga röntgenundersökningar eller spiral-DT-undersökningar och åtta års uppföljning var det tre personer färre som dog på grund av lungcancer. Men det var ändå 15 som dog av lungcancer trots tidig upptäckt, och 250 fick falskt alarm som krävde ytterligare uppföljning. I Sverige tar Socialstyrelsen upp frågan till ny granskning under 2015, för att se om kunskapsläget har förändrats.
Gentester: ibland nyttiga, ofta tvivelaktiga
För inte så länge sedan användes gentester i stort sett bara för att söka efter sällsynta avvikelser i en enda gen, till exempel vid muskelsjukdomen Duchennes muskeldystrofi, som uppträder i barndomen, eller vid Huntingtons sjukdom, en sjukdom i nervsystemet som utvecklas gradvis och som oftast drabbar medelålders personer. Med gentester kan man påvisa de här sjukdomarna. Man kan även testa friska personer som har en familjehistorik som kan tyda på att de löper större risk att utveckla sjukdomen, och även ge råd till dem som planerar att skaffa barn. Men de flesta sjukdomar kan inte spåras till en enda defekt gen. Benägenheten att utveckla en sjukdom har oftast att göra med hur varianter av flera gener påverkar varandra och hur de samverkar med faktorer i miljön. Det är bara när det finns en viss kombination av riskfaktorer i arvsmassan och miljön som sjukdomen bryter ut.[18]
Trots att det oftast är mycket svårt att hänföra sjukdom till en viss genuppsättning, påstår medier och företag, som i många länder marknadsför gentest direkt mot allmänheten, att det är både enkelt och bra att låta göra en genetisk profil. Allt man behöver göra är att skicka in ett salivprov till ett företag som säljer DNA-analyser. De tar betalt och skickar sedan din profil till dig. Men provsvaret kommer knappast att hjälpa vare sig dig eller din läkare att på något rimligt sätt förutsäga risken att du blir sjuk, än mindre vad som eventuellt skulle kunna göras. Sådana här ”gör-det-själv”-metoder uppfyller definitivt inte kriterierna för meningsfull screening (se nedan). Däremot kan resultatet skapa oro och trassla till beslut, men följderna kan också bli mer långtgående, till exempel för andra familjemedlemmar. Som en australisk journalist har uttryckt det: ”För alla som är bekymrade över den smygande medikaliseringen av tillvaron kommer marknaden för gentester definitivt att bryta ny mark, där till synes harmlös teknik bidrar till att förvandla en frisk människa till en rädd patient vars hela identitet omdefinieras av ett antal arvsanlag för sjukdom och tidig död.”[19]
GENERNA ÄR INTE DEN ENDA LEDTRÅDEN
Att agera utifrån kännedom om en enda eller några få genvarianter är som att satsa alla pengar på en enda pokerhand när man bara har sett ett enda kort. Du vet inte vilka andra kort dina arvsanlag har gett dig och inte heller vilken inverkan miljön har. Dessutom handlar det inte bara om fem kort utan om 20 000 gener och tusentals miljöfaktorer. Effekten av en gen kan upphävas av konsekvenserna av livsstil, familjebakgrund och förekomsten av andra, skyddande gener. Många människor bär på defekta gener utan att dessa någonsin leder till sjukdom.”
Sense About science. Making sense of testing: A guide to why scans and other health tests for well people aren’t always a good idea. London: Sense About Science 2008, s. 7. Tillgänglig från: www.senseaboutscience.org
Syftet med screening och varför det behövs vetenskapligt stöd
De exempel vi redan har sett visar att man inte ska ha så bråttom med att sätta igång omfattande massundersökningar. I stället är det värt att stanna upp ett ögonblick, fundera på hur screeningprogrammen är utformade och påminna sig om syftet. De som kallas till sådana undersökningar har inte några symtom på det tillstånd som avses, eller har inte lagt märke till dem, och har inte sökt läkare för detta. Meningen med att massundersöka vissa individer eller grupper i befolkningen är att minska risken att människor ska bli sjuka eller dö i förtid genom att hitta de personer som skulle kunna ha nytta av tidig behandling.[1, 20] Syftet är inte enbart att få tidigare vetskap om att man har en sjukdom – diagnosen i sig behöver ju inte vara till nytta och den kan till och med göra skada.
De viktigaste kriterierna för att avgöra om en screeningundersökning är till nytta beskrevs i en rapport från WHO år 1968.[21] Dessa kriterier har senare omarbetats för att passa dagens hälso- och sjukvårdssystem. Alla som kallas till screening måste få tillräckligt med balanserad information om den undersökning som erbjuds. Det gäller dels de tänkbara riskerna med testet, vilka följderna kan bli och vad testet inte kan visa, dels vilken nytta undersökningen kan göra – så att det är möjligt att fatta ett väl underbyggt beslut.
Man kan sammanfatta de viktigaste punkterna så här: Screening ska bara införas om
- den sjukdom som undersökningen gäller har betydelse för folkhälsan, till exempel för att tillståndet är allvarligt och/eller påverkar många människor
- sjukdomen har ett tidigt stadium som går att upptäcka
- det finns en effektiv och acceptabel behandling, vars effekt sannolikt påverkas av upptäckt via screening
- det finns en tillförlitlig undersökningsmetod som är acceptabel för dem som undersöks
- screeningprogrammet håller hög kvalitet och är värt pengarna i det sammanhang där det ska införas
- den information som ges till dem som inbjuds är opartisk, vetenskapligt välunderbyggd och tydlig med både risker (till exempel för överbehandling) och tänkbar nytta
- inbjudan (kallelsen) till screening inte är tvingande, det vill säga den upplyser om att det går bra att tacka nej
- risken för fysisk eller psykisk skada hos dem som erbjuds screening är mindre än den nytta som de kan ha av den
- det finns goda möjligheter och resurser att diagnostisera och behandla avvikande fynd vid undersökningen.
Detta understryker budskapet i början av kapitlet: beslut om att införa screening måste alltid vara vetenskapligt välunderbyggda. Det ska finnas ett bra faktaunderlag för såväl nytta som risker med undersökningen.
Finns det någon som är normal?
Datortomografi av hela kroppen
I en del länder genomför privata vårdmottagningar helkroppsundersökningar med datortomografi (DT) av huvud, nacke, bröst, buk och bäcken. De erbjuds direkt till allmänheten, vanligen utan att patientens ordinarie allmänläkare konsulteras. Helkroppsundersökningarna marknadsförs ofta som ett sätt att ligga ett steg före en eventuell sjukdom utifrån antagandet att ett ”normalt” resultat på undersökningen är lugnande. Undersökningarna är inte bara dyra – det saknas också vetenskapligt stöd för att det medför hälsovinster att undersöka personer utan symtom eller tecken på sjukdom. Dessutom utsätts individen för en avsevärd stråldos, ungefär 400 gånger så hög som vid en vanlig bröströntgen. Det är så pass mycket att brittiska strålskyddskommittén COMARE (Committee on Medical Aspects of Radiation in the Environment) 2007 utfärdade en stark rekommendation om att ”tjänsteföretag” som erbjuder helkropps-DT till personer som saknar sjukdomssymtom ska upphöra med detta.
År 2010 tillkännagav den brittiska regeringen att man tänkte införa strängare regler för helkroppsundersökningar med DT. Även FDA, den amerikanska motsvarigheten till Läkemedelsverket, har informerat allmänheten om att den typen av undersökningar inte medför någon bevisad nytta, och ger följande kommentar: ”Många människor förstår inte att en helkroppsundersökning med DT inte nödvändigtvis är lugnande som de hoppas eller ger information som kan användas för att förebygga sjukdom. En avvikelse, till exempel, behöver inte vara allvarlig och ett normalt fynd kan vara felaktigt.” [22, 23, 24]
SCREENINGCIRKUSEN
En nyligen pensionerad professor i neurologi hade länge intresserat sig för hur man kan förebygga stroke. År 2009 fick han veta att hans grannar hade fått en broschyr med inbjudan till en screening för stroke och andra komplikationer vid hjärtkärlsjukdom. Broschyren kom från ett privat företag som erbjöd allmänheten ett antal undersökningar som (till en kostnad av 152 pund [cirka 1 650 kronor]) skulle genomföras i en närliggande kyrkolokal. Professorn blev nyfiken, inte minst för att broschyren innehöll en del felaktig information, och bestämde sig för att gå dit själv.
Först var det en undersökning med ultraljud för att söka efter bråck på stora kroppspulsådern. Undersökningen utfördes av en kvinna som inte ville diskutera vad som kunde hända om man hittade ett bråck. Sen var det blodtryck i ben och arm ’för problem med min blodcirkulation’ […] följt av en extra bonus som inte hade med kärlsystemet att göra: undersökning av bentätheten i vristen för att se om jag hade osteoporos [benskörhet]. Sedan följde […] elektrokardiografi (EKG) för att hitta ’problem med hjärtats två förmak’ […] och därefter ultraljudsundersökning av halspulsådern för att se om det fanns någon ’förkalkning på gång’. När jag frågade vilka följder något sådant kunde få, sa de att det kunde bildas blodproppar som skulle kunna leda till stroke. När jag insisterade på att få veta vilken behandling jag skulle kunna få sa de någonting vagt om blodförtunnande medel, men ingenting om operation, inte förrän jag frågade direkt om det också var en möjlighet, och det var det ju. ’Kan det medföra några risker?’ frågade jag oskyldigt. Svaret var att det krävdes en fullständig genomgång av testresultaten för att kunna avgöra det och att jag skulle beställa tid hos min allmänläkare för att diskutera eventuella avvikelser i provsvaren.
Allt detta skedde i en öppen lokal utan avskärmningar (bortsett från undersökningen för pulsåderbråck). Det tycktes inte finnas någon läkare i närheten och personalen var ovillig eller ointresserad av att berätta om följderna av falska alarm eller missade fall, betydelsen av avvikande fynd eller nytta och risker med behandling.
Detta var screening i rent vinstsyfte, varken mer eller mindre. Resultatet skulle landa i mitt knä 21 arbetsdagar senare, och det skulle bli min allmänläkares uppgift att klara ut de känslomässiga och fysiska följderna av eventuella avvikande fynd, sanna eller falska, trots att det inte var hon som hade beställt undersökningarna […] Hela den här screeningcirkusen väcker säkert oro hos känsliga personer, samtidigt som man missar att informera om och ta ansvar för följderna av de avvikelser man upptäcker.”
Warlow C. The new religion: Screening at your parish church. BMJ 2009;338:b1940.
Att kryssa rätt
Det är aldrig lätt att kryssa mellan å ena sidan överdrivet sökande efter sjukdom, och å andra sidan risken att missa tillstånd där tidig upptäckt spelar roll. Ställningstaganden till screeningprogram väcker ofta debatt. Hälso- och sjukvårdssystemen måste hushålla med sina resurser om deras tjänster ska komma hela befolkningen till del. Därför blir utgångspunkten att massundersökningar måste bygga på fast vetenskaplig grund, och nyttan med screeningprogram måste omprövas när kunskapen ökar och omständigheterna förändras. En viktig fråga är om screening bör erbjudas hela segment av befolkningen eller främst dem som löper stor risk för sjukdom.
Källhänvisningar
1 Raffle A, Gray M. Screening: evidence and practice. Oxford: Oxford University Press, rev. repr., 2009.
2 Sense About Science. Making sense of screening. London: Sense About Science, 2009.
3 Goodman MT, Gurney JG, Smith MA, et al. Sympathetic nervous system tumors. In: Ries LAG, Smith MA, Gurney JG, et al (eds). Cancer incidence and survival among children and adolescents: United States SEER Program 1975-1995. National Cancer Institute, SEER Program. NIH Pub. No.99-4649. Bethesda, MD, 1999.
4 Mullassery D, Dominici C, Jesudason EC, et al. Neuroblastoma: contemporary management. Archives of Disease in Childhood – Education and Practice 2009;94:177-85. (Extract)
5 Morris JK. Screening for neuroblastoma in children. Journal of Medical Screening 2002;9:56.
6 Raffle A, Gray M. Screening: evidence and practice. Oxford: Oxford University Press, reviderat nytryck, 2009, pp 89–92.
7 Welch HG. Should I be tested for cancer? Maybe not and here’s why. Berkeley and Los Angeles: University of California Press, 2004, p77.
8 Cosford PA, Leng GC, Thomas J. Screening for abdominal aortic aneurysm. Cochrane Database of Systematic Reviews, 2007, Issue 2, Art. No.: CD002945.
9 Welch HG. Screening mammography – a long run for a short slide? New England Journal of Medicine 2010; 363:1276-8. FIRST 100 WORDS ONLY
Kösters JP, Gøtzsche PC. Regular self-examination or clinical examination for early detection of breast cancer. Cochrane Database of Systematic Reviews 2003, Issue 2. Art. No.: CD003373.
11 Gøtzsche PC, Nielsen M. Screening for breast cancer with mammography. Cochrane Database of Systematic Reviews 2011, Issue 1. Art. No.:CD001877. Note that this review has been updated since it was originally written.
12 Independent UK Panel on Breast Cancer Screening. The benefits and harms of breast cancer screening: an independent review. Lancet 2012;October 30.
13 Cancer Research UK. Prostate cancer – UK incidence statistics. Updated 20 July 2011.
14 Chapman S, Barratt A, Stockler M. Let sleeping dogs lie? What men should know before getting tested for prostate cancer. Sydney: Sydney University Press, 2010.
15 Holmström B, Johansson M, Bergh A, et al. Prostate specific antigen for early detection of prostate cancer: longitudinal study. BMJ 2009;339:b3537.
16 Djulbegovic M, Beyth RJ, Neuberger MM, et al. Screening for prostate cancer: systematic review and meta-analysis of randomised controlled trials. BMJ 2010;341:c4543.
17 Stark JR, Mucci L, Rothman KJ, et al. Prostate cancer screening: the controversy continues. BMJ 2009;339:b3601.
18 National Cancer Institute. Lung cancer trial results show mortality benefit with low-dose CT. Pressrelase, 11 April 2010.
19Moynihan R. Beware the fortune tellers peddling genetic tests. BMJ 2010;341:c7233.
20 Thornton H. The screening debates: time for a broader approach? European Journal of Cancer 2003;39:1807-9.
21 Adapted from Wilson JMG, Jungner G. Principles and practice of screening for disease. Public health paper no 34. Geneva: World Health Organization, 1968.
22 COMARE 12th Report: The impact of personally initiated X-ray computed tomography scanning for the health assessment of asymptomatic individuals. Press release, 19 December 2007.
23 Department of Health. Better protection for patients having ‘MOT’ scans. 2010.
24 Food and Drug Administration. Radiation-emitting products: Computed tomography and full-body CT scans – what you need to know.
